LEYES DE LOS GASES
- CyRE CURSOS Y REGULARIZACIÓN ESTUDIANTIL
- 29 jul
- 2 Min. de lectura
LEYES DE LOS GASES








EJERCICIOS
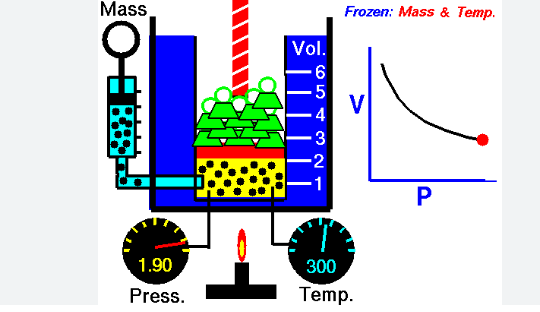
1. (Boyle – presión y volumen a T constante)
Un gas ocupa 5.0 L a 1.2 atm. ¿Cuál será su volumen si la presión aumenta a 3.0 atm, manteniendo la temperatura constante?
2. (Charles – volumen y temperatura a P constante)
Un gas tiene un volumen de 3.0 L a 273 K. ¿Qué volumen tendrá a 546 K si la presión se mantiene constante?
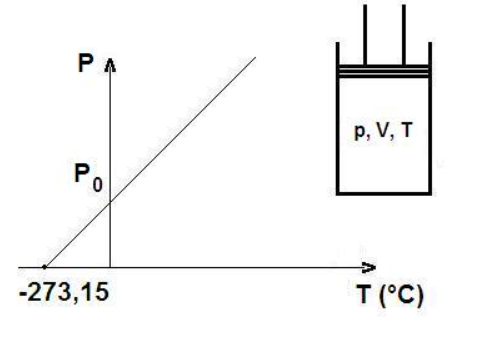
3. (Gay-Lussac – presión y temperatura a V constante)
Un gas tiene una presión de 1.0 atm a 300 K. ¿Qué presión tendrá si se calienta a 450 K y el volumen no cambia?
4. (Boyle)
A temperatura constante, un gas a 2.0 atm ocupa 8.0 L. ¿Cuál será su presión si se comprime a 4.0 L?
5. (Charles)
Un gas ocupa 1.5 L a 200 K. ¿Cuál será su volumen a 400 K manteniendo constante la presión?
6. (Gay-Lussac)
Un gas tiene una presión de 4.0 atm a 250 K. Si se enfría a 125 K a volumen constante, ¿cuál será su nueva presión?
7. (Ley General del Estado Gaseoso)
Un gas tiene un volumen de 2.0 L a 1.0 atm y 300 K. ¿Cuál será su volumen si la presión cambia a 2.0 atm y la temperatura a 600 K?
8. (Boyle)
Un gas a temperatura constante tiene un volumen inicial de 10.0 L y una presión de 0.8 atm. ¿Cuál será la presión si el volumen disminuye a 2.0 L?
9. (Charles)
El volumen de un gas es 2.5 L a 250 K. ¿A qué temperatura estará el gas si su volumen se incrementa a 5.0 L a presión constante?
10. (Ley General del Estado Gaseoso)
Un gas ocupa 6.0 L a 1.2 atm y 350 K. ¿Qué volumen ocupará si se lleva a 2.4 atm y 700 K?
RESPUESTAS






Comentarios